Ковалентная связь
Во всех молекулах атомы связаны между собой ковалентными связями. Ковалентная связь образуется в месте перекрывания электронных облаков обоих атомов.
Рассмотрим образование ковалентной связи на примере молекулы водорода. У каждого атома водорода на внешнем (первом)

электронном слое находится по одному электрону. Следовательно, до завершения этого слоя не хватает одного электрона. При сближении атомов, ядро каждого из них притягивает к себе электронное облако другого. В результате облака обоих атомов проникают друг в друга или перекрываются так, что между ядрами возникает область повышенного отрицательного заряда, которую обычно называют областью повышенной электронной плотности. Ядра атомов притягиваются к этой области до тех пор, пока не наступит равновесие между силами межъядерного отталкивания и силами притяжения. Между атомами возникает прочное взаимодействие, которое и называется химической связью.
Каждый атом получил недостающий электрон до завершения своего энергетического уровня. При этом электроны, участвующие в образовании связи принадлежат обоим атомам, т.е. образуют общую электронную пару.
Схематически образование молекулы водорода можно изобразить так:
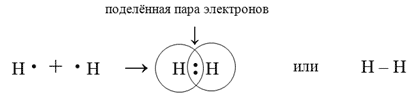 Точками на схемах при химическом знаке элемента обозначаются электроны внешнего электронного слоя, а двумя точками в формуле — пара электронов. Такие формулы, в которых изображаются все электроны внешних электронных слоев атомов, называют электронными формулами. Обобществленная пара электронов (спаренные электроны) обычно изображается в виде черточки, например: H—H
Точками на схемах при химическом знаке элемента обозначаются электроны внешнего электронного слоя, а двумя точками в формуле — пара электронов. Такие формулы, в которых изображаются все электроны внешних электронных слоев атомов, называют электронными формулами. Обобществленная пара электронов (спаренные электроны) обычно изображается в виде черточки, например: H—H
Эта черточка обозначает ковалентную связь.
Ковалентная связь возникает между атомами неметаллов.

Рассмотрим образование более сложной молекулы хлора F2. У фтора 7 электронов на внешнем слое, 1 неспаренный электрон образует общую электронную пару.
Черточка на схемах строения молекул обозначает всегда пару электронов. Такие схемы часто называют графическими или структурными формулами. Графическая формула молекулы водорода вам уже известна: Н — Н

Если атомы соединены между собой с помощью одной общей электронной пары, то такая ковалентная связь называется одинарной. Но между двумя атомами может возникать и большее число связей. В таких случаях говорят о кратности связи.
Например, атомам кислорода, элемента VIA-группы, до завершения внешнего электронного слоя необходимо 2 электрона. Поэтому 2 атома кислорода при образовании молекулы O2 обобществляют уже не одну, а две пары электронов. Они связываются между собой двойной ковалентной связью, как показано в электронной формуле молекулы кислорода O2.
В молекуле азота N2 атомы связаны между собой тройной ковалентной связь. У каждого атома остается по одной паре электронов на внешнем слое. Чем больше общих электронных пар связывают два атома между собой, тем меньше расстояние между их ядрами, тем прочнее образовавшаяся химическая связь в молекуле. Например, связь между атомами кислорода в молекуле кислорода О = О более короткая и более прочная, чем в молекуле пероксида водорода: H – O – O – H, так как она образована двумя общими электронными парами.
Особенности ковалентной связи:
1.образуется среди неметаллов;
2.образуется общая электронная пара.
Решите самостоятельно: только ковалентные связи имеет каждое из двух веществ:
- Na, H2
- K, Cl2
- Al, O2
- O2, Cl2
